A reportagem principal da revista Época de no 680, entitulada “A saúde da Dilma”, revela que a presidente tem tireóide de hashimoto. Em virtude da compatibilidade dessa informação com o assunto do nosso blog, vamos explicar melhor o que vem a ser essa doença
A tireóide de Hashimoto recebeu este nome em homenagem ao médico que a descobriu, o doutor Hakaru Hashimoto, em 1912. Trata-se de uma doença auto-imune, sendo a causa mais comum de hipotireoidismo nos EUA. Apesar de estar muito associada a casos de hipotireoidismo, os dois termos não são intercambiáveis. A tireóide de Hashimoto é uma doença que pode ter diversos sintomas ou mesmo permanecer assintomática por muitos anos, enquanto que o hipotireoidismo é uma condição clínica de baixa atividade da glândula tireóide.
Muitas vezes, pacientes com tireoide de Hashimoto são assintomáticos durante a maior parte de vida, só vindo a desenvolver a doença já em idade adulta.Os sintomas mais comuns são aumento no tamanho da glândula tireóide, depressão, fatiga, ganho de peso, constipação, queda de cabelos, problemas de fertilidade e dores nas articulações e nos músculos. É importante frisar que na doença de Hashimoto pode haver momentos em que a atividade da tireóide é aumentada após períodos de hipotireoidismo, havendo alternância entre sintomas de hiper e hipotireoidismo.No caso da presidente Dilma, a tireóide de Hashimoto levou a um quadro de hipotireoidismo, como informa a reportagem.
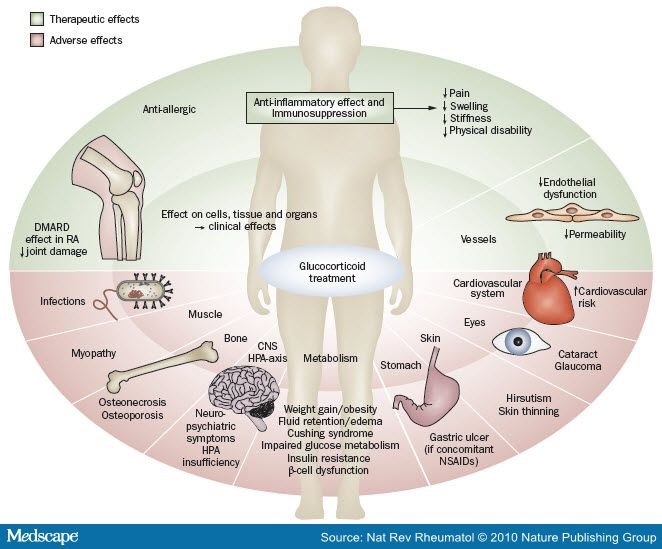
A tireóide de Hashimoto não tem cura, mas o hipotireoidismo por ela gerado pode ser controlado com a reposição de T3 e T4. O remédio usado pela presidente, o Synthroid, é na verdade o hormônio T4 (levotiroxina de sódio) produzido artificialmente. Se houver desenvolvimento de inflamações na tireóide, é comum o uso conjunto de corticóides(que são poderosos anti-inflamatórios, como já citado).
Molécula da levotiroxina de sódio, componente ativo do Synthroid, o remédio usado pela Dilma.
O diagnostico da tireóide da Hashimoto é feito de diversas formas. Pode-se realizar exames de sangue para detector primeiramente o hipotireoidismo. Taxas baixas de T3 e T4, ou taxas altas de TSH revelam quadros de hipotireoidismo. As taxas altas de TSH(hôrmio estimuante da tireóide) são uma tentativa de hipófise de equilibrar a baixa produção de T3 e T4, sendo típica do período inicial de desenvolvimento do hipotireoidismo. Se detectado o hipotireoidismo, deve ser feito um exame extra para detectar as taxas de anticorpos contra tireoglobulina e contra a tireóide peroxidase, as duas principais enzimas da tireoide. Se essas taxas se apresentarem elevadas, trata-se de um quadro de tireóide de Hashimoto que levou a um hipotireoidismo.
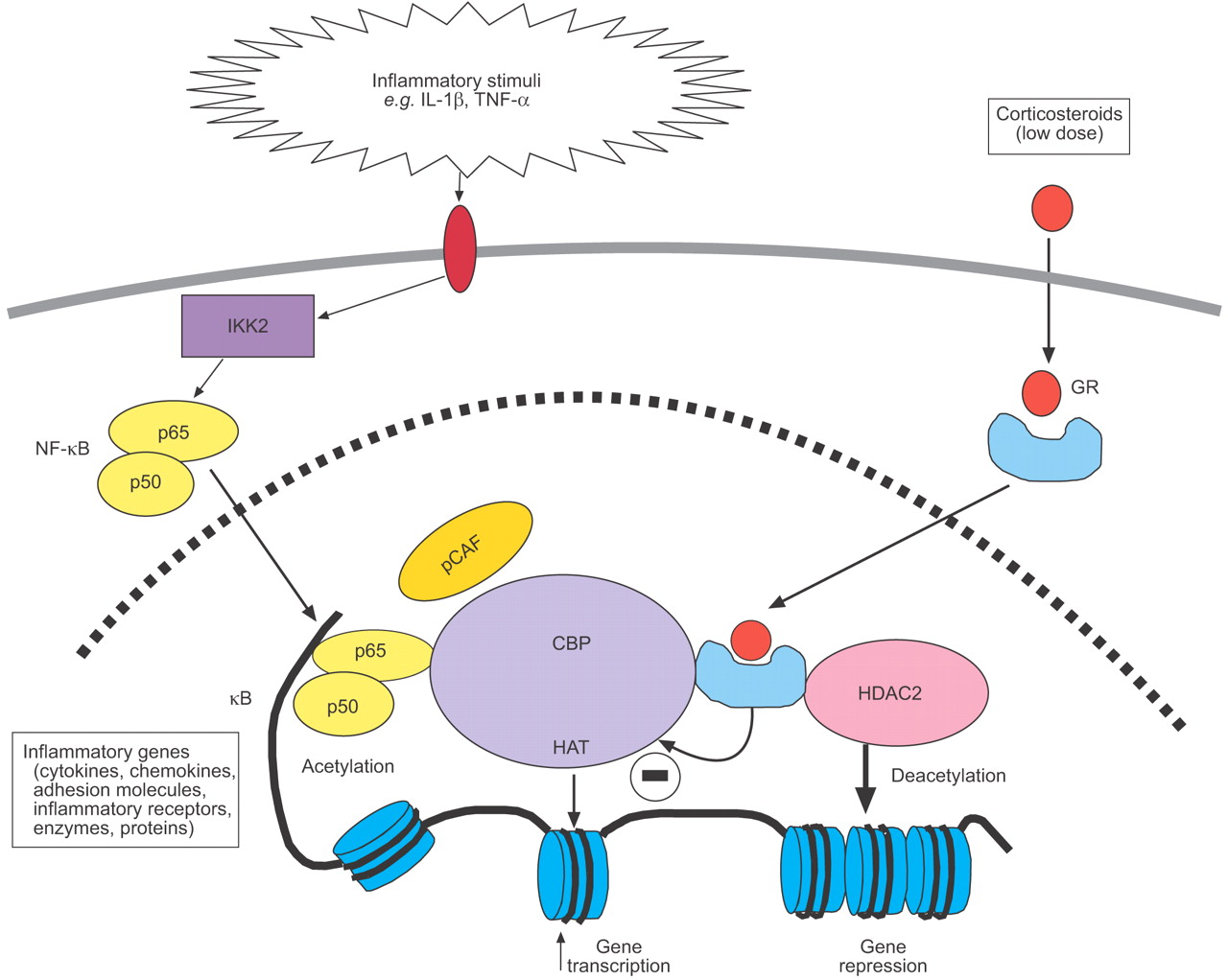
O outro medicamento utilizado no tratamento da presidente foi o Calcort, um corticóide, que tem por princípio ativo o deflazacorte. Esse medicamento tem ação anti-inflamtória, sendo usado no controle de respostas alérgicas exageradas, inflamações de pulmão e de articulações. Além disso, esse medicamento também atua reduzindo o número de certas “células brancas”do sistema imune, sendo muito utilizado no tratamento de doenças autoimunes e de certos tipos de câncer, como linfomas a leucemia.
No caso, a utilização mais recente desse medicamento pela presidente foi contra um quadro de pneumonia, provavelmente para reduzir inflamações no pulmão. No entanto, é possível que o mesmo medicamento tenha sido usado anteriormente contra o linfoma(câncer nos nódulos linfáticos) ou contra a tireóide de Hashimoto(que é uma doença auto-imune).
Além disso, foi citado que a pesidente faz uso do slow-K, um medicamento a base de cloreto de potássio utilizado para aumentar os níveis de potássio no sangue. Baixos níveis de potássio no sangue podem estar relacionados a uma atividade alta da glândula adrenal, sobretudo a região produtora de mineralocorticóides. Os mineralocorticóides, principalmente a aldosterona, atuam aumentando a eliminação de potássio e a reabsorsão de sódio. Assim, uma produção acentuada desse hormônio pode levar a uma baixa de potássio, o que é corrigido usando-se o slow-K.
Por Daniela Frank de Albuquerque
Bibliografia:
www.medicinenet.com/hashimotos_thyroiditis/article.htm
thyroid.about.com/cs/hypothyroidism/a/hashivshypo.htm
http://emedicine.medscape.com/article/120937
www.netdoctor.co.uk/medicines/100000429.html
www.rxlist.com/synthroid-drug.htm